Online adatszolgáltatási kötelezettség
Külföldi vállalkozások esetén lehetőség vagy kötelezettség az online adatszolgáltatás?
A francia egészségügyi minisztérium egyelőre nem árulja el, melyik cég milyen gyógyszerének tesztje járt végzetes következményekkel Franciaország nyugati részén. Meg nem erősített hírek szerint egy kannabinoid tartalmú fájdalomcsillapítót teszteltek. A tárca azt elismerte, hogy a kísérletben résztvevők közül egy ember agyhalott lett, öten pedig súlyos állapotba kerültek – derült ki a Reuters tudósításából.
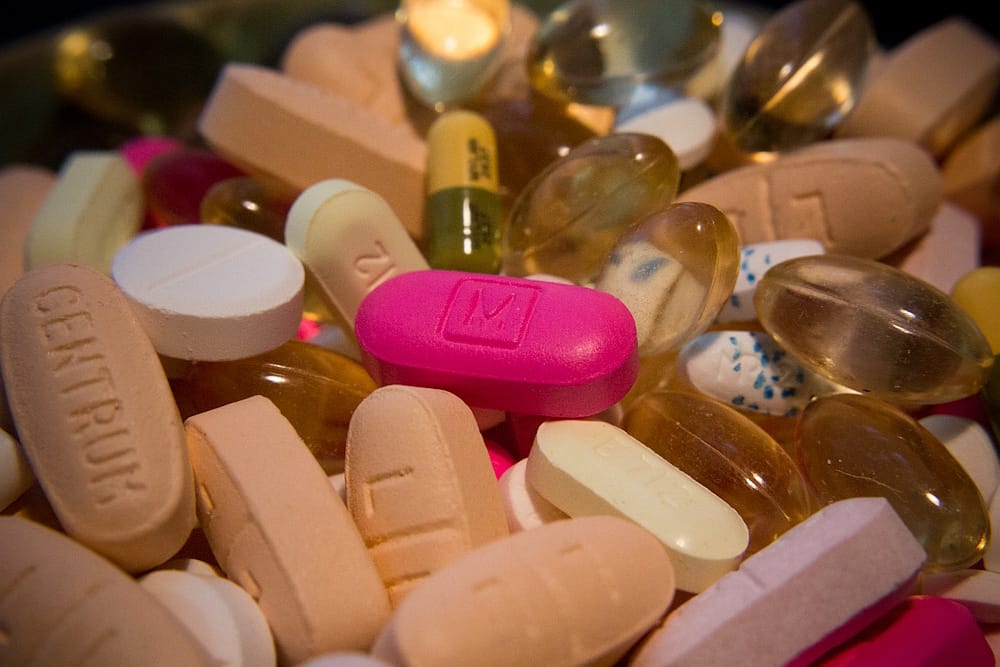
A francia egészségügyi minisztérium nemcsak a kísérleti gyógyszert, hanem a tesztet végző céget sem nevezte meg. Csak annyit mondtak, hogy a készítményt egy európai laboratóriumban fejlesztették ki. Emellett azt erősítették meg, hogy az egyik kísérleti alany a szertől agyhalott lett, őt hétfő vitték kórházba Rennes-ben. A többi, súlyos állapotban lévő beteg szerdán illetve csütörtökön került kórházba. Hat önkéntesnek nem esett baja a gyógyszer bevétele után.
A Reuters egyik informátora szerint egy kannabinoid tartalmú fájdalomcsillapítót teszteltek. Orális, vagyis szájon át adandó készítményről van szó, a pontos gyógyszerforma nem ismert.
A nagy-britanniai GW Pharma foglalkozik kannabinoid tartalmú gyógyszerekkel, amelyet szklerózis multiplexes betegeknek adnak a remegéssel, görcsöléssel járó állapot csökkentésére. A társaságnak azonban nincs köze a franciaországi esethez.
A franciaországi tesztet felfüggesztették, és minden önkéntest, aki részt vett a kísérletben, visszahívták felülvizsgálatra.
Az Európai Gyógyszerügynökség (EMA) szóvivője Londonból azt nyilatkozta, hogy egyelőre nem jutott el hozzájuk minden szükséges információ a francia esetről, de figyelemmel kísérik azt.
A klinika fázisban lévő gyógyszerkísérleteknél természetesen előfordulhatnak nem várt eredmények, de szakemberek szerint ritkán történik olyan súlyos probléma, mint Franciaországban. Legutóbb 2006-ban, Londonban került hat kísérleti alany intenzív osztályra, miután egy tesztelés alatt álló gyógyszerből kaptak. Volt köztük olyan, akinek a következmények miatt ujjperceit és lábujjait kellett amputálni.
A Reuters jelentésében emlékeztetnek, hogy a gyógyszerkísérleteknél az 1-es klinikai fázisban egészséges önkénteseken tesztelik az adott készítményeket. Itt próbálják felmérni a szervezet reakciót az adott hatóanyagra, valamint azt, milyen lehet a megfelelő dozírozás. Ha ezek a tesztek az előírásoknak megfelelően végződnek, jön a II-es, majd a III-as fázis: ezekben próbálják felmérni a gyógyszer hatásosságát és biztonságosságát. Ha itt is sikerül teljesíteni minden előírást, a megfelelő engedélyezési folyamat után kerülhet a gyógyszer forgalomba.
Külföldi vállalkozások esetén lehetőség vagy kötelezettség az online adatszolgáltatás?
Hogyan és mikor lehet elrendelni a rendkívüli munkavégzést?
Óriási már a zaj a közösségi médiában. Érdemes még pénzt költeni a tartalommarketingre? Hogyan lehet ezt jól csinálni?
Az ingatlan bérleti díja és a kapcsolódó költségek elszámolhatók a költségként? Milyen járulékokat kell fizetni?