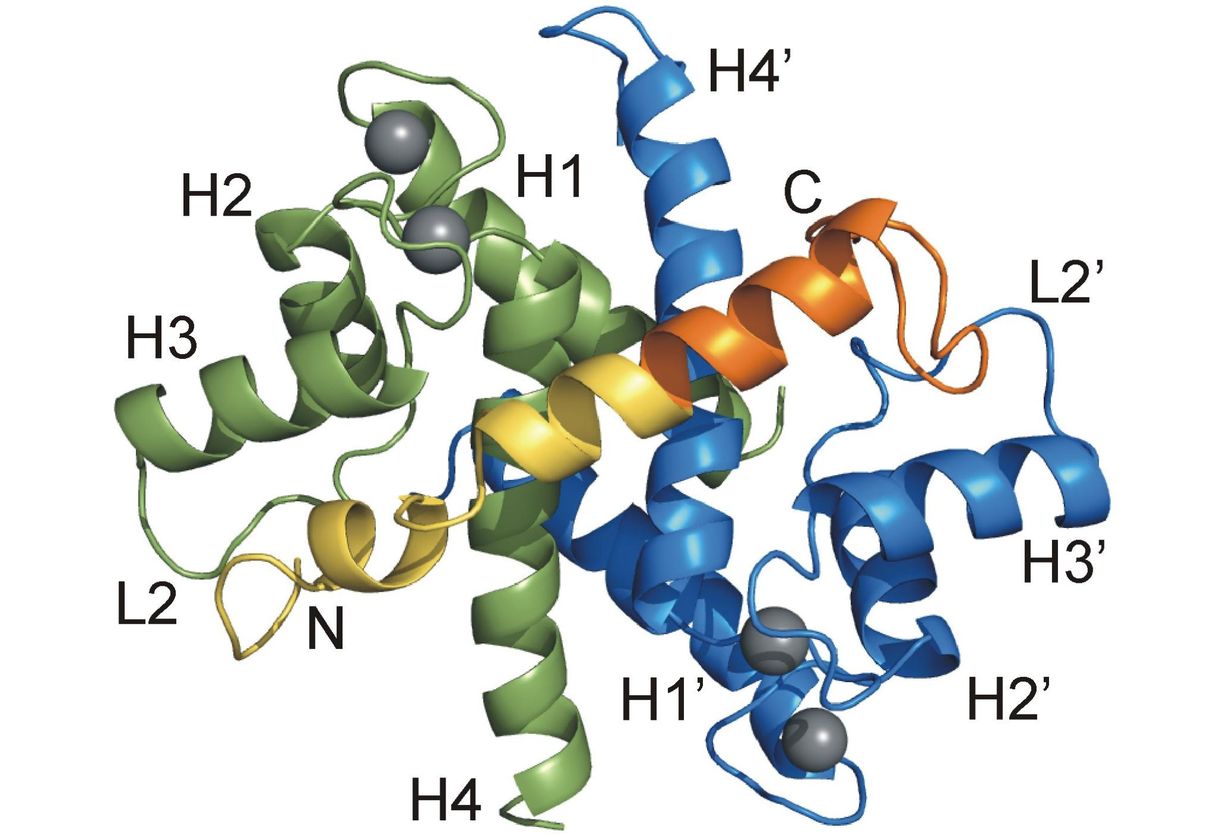
Az S100A4 - korábbi nevén metasztazin -, aktív szerepet játszik tumor áttétek képződésében, valamint a reumás ízületi gyulladás kialakulásában. Korábban kimutatták, hogy a metasztazin-szint emelkedése fokozza a sejtek migrációs képességét, méghozzá érdekes módon úgy, hogy szabályozza az egyik nem-izom miozin forma által kialakított filamentumokat. Az viszont eddig ismeretlen volt, hogy milyen módon kötődik az S100A4 a miozin farokrészéhez és miként esnek szét a miozin filamentumok a kötődés hatására.
 Az ELTE-s kutatócsoportnak sikerült az S100A4 és egy miozin peptid komplexének atomi felbontású szerkezetét meghatározni és magyarázatot adni a miozin filamentum szétesés mechanizmusára. Korábban is felvetődött, hogy az S100A4 gyógyszer-célpont fehérje lehet, de az eddigi kísérleteket nehezítette, hogy nem volt ismert az S100A4 és a hozzá kötődő fehérjék nagyfelbontású szerkezete. A szerkezet ismeretében lehetőség nyílhat olyan molekulák keresésére és tervezésére, amelyek az S100A4-miozin kölcsönhatás gátlásán keresztül a tumor metasztázisok és a reumatoid artritisz kezelésére alkalmas gyógyszerré fejleszthetők. Az ELTE-munkacsoport alkalmazott kutatási együttműködést tervez egy magyarországi biotechnológiai céggel a fenti elképzelés megvalósítására.
Az ELTE-s kutatócsoportnak sikerült az S100A4 és egy miozin peptid komplexének atomi felbontású szerkezetét meghatározni és magyarázatot adni a miozin filamentum szétesés mechanizmusára. Korábban is felvetődött, hogy az S100A4 gyógyszer-célpont fehérje lehet, de az eddigi kísérleteket nehezítette, hogy nem volt ismert az S100A4 és a hozzá kötődő fehérjék nagyfelbontású szerkezete. A szerkezet ismeretében lehetőség nyílhat olyan molekulák keresésére és tervezésére, amelyek az S100A4-miozin kölcsönhatás gátlásán keresztül a tumor metasztázisok és a reumatoid artritisz kezelésére alkalmas gyógyszerré fejleszthetők. Az ELTE-munkacsoport alkalmazott kutatási együttműködést tervez egy magyarországi biotechnológiai céggel a fenti elképzelés megvalósítására.
A kísérleti munka nagy részét Kiss Bence PhD-hallgató végezte Nyitray László, a Természettudományi Kar Biokémiai Tanszék vezetőjének kutatócsoportjában, együttműködésben a Göteborgi Egyetem Kémiai és Molekuláris Biológiai Tanszékén Katona Gergely kutatócsoportjával. A kutatás az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósul meg (a támogatás száma TÁMOP 4.2.1/B-09/1/KMR-2010-0003).

ELTE
A kísérleti munka nagy részét Kiss Bence PhD-hallgató végezte Nyitray László, a Természettudományi Kar Biokémiai Tanszék vezetőjének kutatócsoportjában, együttműködésben a Göteborgi Egyetem Kémiai és Molekuláris Biológiai Tanszékén Katona Gergely kutatócsoportjával. A kutatás az Európai Unió támogatásával, az Európai Szociális Alap társfinanszírozásával valósul meg (a támogatás száma TÁMOP 4.2.1/B-09/1/KMR-2010-0003).